[Paper: Mean-field and linear regime approach to magnetic hyperthermia of core-shell nanoparticles: can tiny nanostructures fight cancer? Marcus S. Carrião, Andris F. Bakuzis. Nanoscale, 2016,8, 8363-8377. DOI: 10.1039/C5NR09093H]

Hyperthermia, for cancer treatment, is induced by increasing the temperature to activate tumor cell death. This high temperature can be created by introducing nanoparticles into the tumor that function as heaters, and after their function is completed they are eliminated by the body. Magnetic nanoparticles may be used in these treatments because they have the ability to generate heat when subjected to alternating magnetic fields of specific intensity and frequency.
A work on nanomedicine (nanotechnology used in medicine) fully conducted at the Brazilian Federal University of Goiás (UFG) suggests a new strategy using hyperthermia for cancer treatment: using smaller magnetic nanoparticles than those normally used and composed of more than one material, which could provide several advantages to the patient. To reach this conclusion, the researchers developed an innovative theoretical method that paves the way for manufacturing magnetic nanoparticles optimized for hyperthermia. The study was reported in a paper published in the prestigious Nanoscale journal, signed by the doctoral student Marcus Carrião dos Santos and his supervisor Andris Figueiroa Bakuzis, professor at the Physics Institute of UFG.
Hyperthermia cancer treatment generally uses nanoparticles that are relatively large (20 nm size range) and homogeneous (from a single material), which are considered as the most effective to generate heat according to theoretical studies based on traditional methods. However, these “large” nanoparticles accumulate quickly in the liver and it may take several months or years for these particles to leave the body of the patient being treated. On the other hand, nanoparticles smaller than 10 nm are rapidly eliminated in the urine, reducing the possibilities of intoxication and thereby increasing the selection of materials that can be used to manufacture them.
The relationship between particle size and excretion route (liver or kidney) was a conclusion reached by Bakuzis and colleagues from evidence reported in the scientific literature and pre-clinical studies (in vivo) carried out within a multidisciplinary research network, coordinated by Bakuzis, and aimed at solving problems associated with the use of magnetic nanoparticles for cancer treatment.
In addition, smaller nanoparticles have better distribution and penetration in tumors, among other advantages in the context of cancer treatment.
Aware of these characteristics, Bakuzis and dos Santos investigated the possibility of manufacturing nanoparticles of less than 10 nm that could efficiently generate heat. An important insight came from an article published in 2011 in the Nature Nanotechnology journal (Nat. Nanotech. 6, 418 (2011)). Professor Bakuzis says that “in this article, the researchers concluded experimentally that certain heterogeneous (from different materials) core-shell structures of spinel ferrites warmed more efficiently than homogeneous particles”.
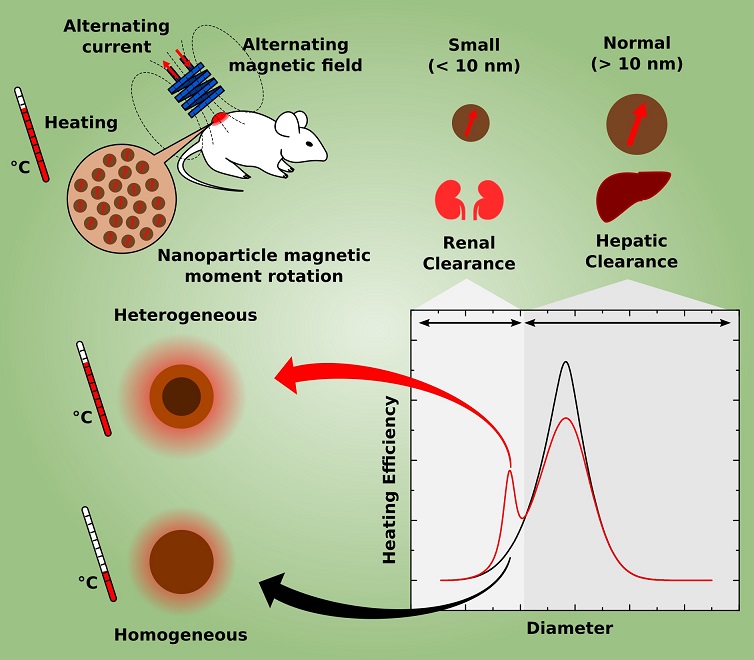
The pair of scientists then decided to theoretically investigate whether nanoparticles less than 10 nm formed by one material core and a shell of another material could efficiently generate heat and how to optimize them for this function. However, the conventional methods available for this modeling were not adequate. In fact, they considered the nanoparticle as a homogeneous entity, ignoring the fact that the surface atoms and the core atoms respond differently to the application of a magnetic field. This oversight became more significant in the study of particularly heterogeneous particles such as those they intended to study, the reason why the researchers from Goiás decided to develop a more suitable model for the study object. Bakuzis explains that “in the paper we presented the first analytical hyperthermia model of core-shell nanoparticles within the linear response and mean-field theory, and from these calculations we pointed out important materials properties to achieve efficient heat generation.”
The results obtained by the physicists and published in the paper may have a significant impact in a health issue that concerns humanity, cancer cure. “Our studies indicate that it is possible to develop small particles for cancer treatment that can be quickly eliminated from the body via the kidneys. In particular, by combining different materials in the nanostructure”, summarizes Bakuzis.
To work with impact on this interface theme, Bakuzis is always in contact with a pool of knowledge of various areas. In addition to leading the multidisciplinary nanomedicine network that includes researchers with backgrounds in tumor biology, genetics, physiology, pharmacy, veterinary medicine, biophysics, physics, medical physics and chemistry, the professor and his group actively participate in scientific events that bring together many different professionals, including doctors with various specializations already using hyperthermia in humans for cancer treatment. “These scientific contacts are fundamental in interface areas such as the one our group works with,” concludes Bakuzis.
The research that led to the paper in the Nanoscale journal received funding from the Brazilian National Scientific and Technological Development Council (CNPq) and from the Research Foundation of the State of Goiás (FAPEG) and was carried out as part of the doctoral work of Marcus Carrião dos Santos.

PAULO HENRIQUE DIAS
Parabéns a todos os envolvidos nestas pesquisas, sem sombra de dúvidas estão no caminho certo, gostaria de saber se já existe algum centro realizando esse tratamento no Brasil, e se não o que seria preciso para começar.
Andris Bakuzis
Prezado Ebert
Obrigado pelas observações e perguntas. Na literatura costuma-se ouvir que ao chegar em determinada temperatura pode-se aniquilar células tumorais. No entanto, a situação é mais complexa. De fato pesquisadores desta área, Medicina Térmica, já sabem que o relevante é o que chamamos de dose térmica. Neste caso não só a temperatura mas o tempo de permanência nesta temperatura, que é relevante para o tratamento por meio de entrega de calor.
Dito isto, talvez seja importante comentar que pode-se localizar radiação eletromagnética (não-ionizante) em órgãos específicos ou pequenas regiões (mas infelizmente até o momento não em qualquer região do corpo). Algumas estratégias invasivas, como equipamentos de ablação por RF ou microondas, já estão em uso na medicina há algum tempo.
Por outro lado, equipamentos que fazem esta entrega de forma não-invasiva também já foram aprovados pela FDA para uso em seres humanos, seja para tratar tumores superficiais (sem uso de nanotecnologia), ou ainda outros, como um recente desenvolvimento de uma empresa européia, que possui um equipamento que consegue localizar num volume de interesse campos magnéticos capazes de, ao interagir com nanopartículas magnéticas, gerar calor suficiente para auxiliar no tratamento do câncer. Este equipamento está aprovado para uso em conjunto, i.e. a braquiterapia e hipertermia no tratamento de tumores do cérebro.
Esta terapia conjunta, aonde calor é associado a radioterapia (ou quimioterapia), pode sim auxiliar na diminuição de efeitos colaterais. Na verdade já se sabe por meio de estudos clínicos e pré-clínicos, que a dose pode reduzir consideravelmente ao se combinar calor a terapias tradicionais.
Portanto, é muito provável que no futuro próximo, além das terapias tradicionais outras estratégias, como esta de entrega de calor, possam ser acopladas de maneira mais usual para melhorar a qualidade de vida de pacientes com câncer.
Ebert Ribeiro Figueiroa
Se altas temperaturas podem causar câncer, como em bebidas acima de 60 graus centígrados, que temperatura seria a adequada para dissolução de tumores e como regular essa temperatura através dessas nanoparticulas, já que os meios, em diferentes partes do corpo, são diferentes? Todo trabalho que está sendo feito merece todos os esforços destes profissionais que estão trabalhando em conjunto para quem sabe uma possível cura para o câncer, que até a pouco, seria uma missão que quase impossível. Será? Este poderá ser a resposta e sem efeitos colaterais que acompanham a maior parte dessas terapias. Parabéns por todos estarem proporcionando mais esta esperança a comunidade.
Andris Bakuzis
Prezado Ebert
Notei agora também que esqueci de responder outra questão relevante apontada por você, a qual diz respeito a monitorar a temperatura dentro dos órgãos de maneira não-invasiva. Esta área de monitoramento da entrega de calor é muito importante neste tipo de tratamento. Atualmente, pode-se utilizar a técnica de ressonância magnética (RMNI) para monitorar tridimensionalmente esta entrega de calor na região de interesse (é possível usar também o ultrassom mas ainda parecem haver algumas limitações neste caso). Infelizmente, no caso das nanopartículas magnéticas, tal estratégia não pode ser usada, já que o calor depende da rotação dos momentos magnéticos das nanopartículas. Estas, por sua vez, dentro de um equipamento de RMNI, encontram-se de certa forma bloqueadas, já que o paciente entra dentro de um magneto permanente, ou seja há um campo magnético de alta intensidade dentro do RMNI que impede que sob ação de um campo oscilante haja rotação dos seus momentos magnéticos. Portanto, impossibilita a geração de calor. Novas alternativas não-invasivas estão sendo pensadas para resolver esta questão, mas até o momento no tratamento de pacientes, isto ainda é feito majoritariamente por meio da inserção de termômetros de fibra óptica no paciente.