O artigo científico com participação de membros da comunidade brasileira de pesquisa em Materiais em destaque neste mês é: Mean-field and linear regime approach to magnetic hyperthermia of core-shell nanoparticles: can tiny nanostructures fight cancer? Marcus S. Carrião, Andris F. Bakuzis. Nanoscale, 2016,8, 8363-8377. DOI: 10.1039/C5NR09093H.

A hipertermia, enquanto tratamento do câncer, é um aumento de temperatura capaz de acionar processos de morte nas células tumorais. Uma das vias para gerar essa alta temperatura é a introdução nos tumores de nanopartículas que funcionam como aquecedores e, depois de cumprirem com a sua função, são eliminadas pelo organismo. Nanopartículas magnéticas podem ser utilizadas nesses tratamentos por terem a capacidade de gerar calor quando submetidas a um campo magnético oscilante de intensidade e frequência adequadas.
Um trabalho de nanomedicina (nanotecnologia para uso em medicina) totalmente realizado na Universidade Federal de Goiás (UFG) sugere uma nova estratégia para o tratamento do câncer por meio de hipertermia: utilizar nanopartículas magnéticas menores do que as normalmente usadas e compostas por mais de um material, as quais apresentariam uma série de vantagens para o paciente. Para chegar nessa conclusão, os autores da pesquisa desenvolveram um método teórico inovador que aponta caminhos para a fabricação de nanopartículas magnéticas do tipo proposto, otimizadas para a hipertermia. O estudo foi reportado num artigo publicado no prestigiado periódico Nanoscale, assinado pelo doutorando Marcus Carrião dos Santos e seu orientador Andris Figueiroa Bakuzis, professor do Instituto de Física da UFG.
Em geral, tratamentos do câncer por hipertermia utilizam nanopartículas homogêneas (feitas de um único material) relativamente grandes, da ordem de 20 nm, que são consideradas as mais eficientes na geração de calor de acordo com estudos baseados em métodos teóricos tradicionais. Entretanto, essas nanopartículas “grandes” se acumulam rapidamente no fígado e podem levar vários meses, e até anos, para sair do organismo do paciente em tratamento. Por sua vez, as nanopartículas menores de 10 nm são eliminadas rapidamente pela urina, diminuindo as possibilidades de intoxicação e, assim, ampliando as opções de materiais que podem ser usados para fabricá-las.
A relação entre o tamanho das partículas e a via de excreção (hepática ou renal) foi uma conclusão à qual Bakuzis e seus colaboradores chegaram a partir de evidências reportadas na literatura científica e de estudos pré-clínicos (in vivo) realizados no contexto de uma rede de pesquisa multidisciplinar, coordenada por Bakuzis, dedicada a resolver problemas associados à utilização de nanopartículas magnéticas para o tratamento do câncer.
Além disso, nanopartículas menores apresentam melhor distribuição e penetração nos tumores, entre outras vantagens no contexto do tratamento do câncer.
Cientes dessas características, Bakuzis e dos Santos pesquisaram a possibilidade de fabricar nanopartículas de menos de 10 nm que conseguissem gerar calor com eficiência. Uma importante inspiração veio de um artigo publicado em 2011 na revista científica Nature Nanotechnology (Nat. Nanotech. 6, 418 (2011)). “Neste artigo os pesquisadores concluíram experimentalmente que determinadas estruturas core-shell heterogêneas (feitas de materiais distintos) a base de ferritas do tipo espinélio aqueciam de forma mais eficiente que partículas homogêneas”, relata o professor Bakuzis.
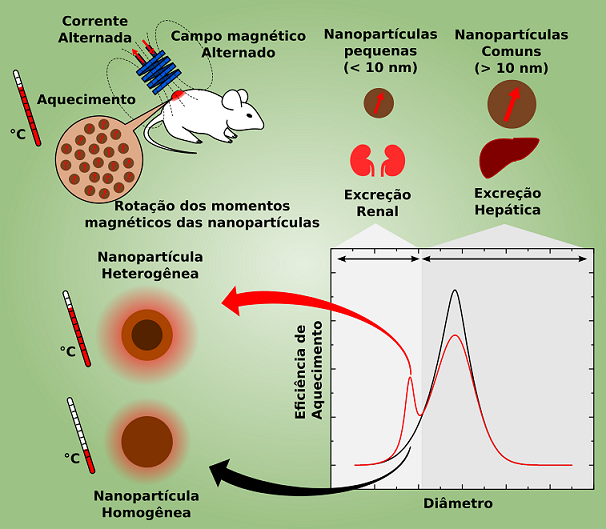
A dupla de cientistas decidiu então estudar teoricamente se nanopartículas de menos de 10 nm formadas por um núcleo de um material e uma casca de outro material poderiam gerar calor de maneira eficiente e como otimizá-las para essa função. Entretanto, os métodos convencionais disponíveis para fazer essa modelagem não eram adequados. De fato, eles consideravam a nanopartícula como uma entidade homogênea, desprezando o fato de que os átomos da superfície e os do núcleo respondem diferentemente à aplicação do campo magnético. Essa omissão tornava-se mais significativa no caso do estudo de partículas particularmente heterogêneas como aquelas que a dupla pretendia estudar, motivo pelo qual os pesquisadores de Goiás encararam o desenvolvimento de um modelo mais adequado ao objeto de estudo. “No artigo apresentamos o primeiro modelo analítico de hipertermia em nanopartículas core-shell dentro da teoria de resposta linear e campo médio, e, a partir destes cálculos, apontamos importantes propriedades de materiais para alcançar uma geração de calor eficiente”, diz Bakuzis.
Os resultados publicados no artigo, obtidos por dois cientistas formados em física, poderão ter um impacto significativo num tema do campo da saúde que preocupa a humanidade, a cura do câncer. “Nossos estudos indicam que é possível desenvolver partículas pequenas para o tratamento oncológico que possam ser eliminadas rapidamente do corpo por meio desta rota renal. Em particular, por meio da combinação de diferentes materiais na nanoestrutura”, resume Bakuzis.
Para trabalhar com impacto nesse tema de interface, Bakuzis está sempre em contato com conhecimento de diversas áreas. Além de liderar a rede multidisciplinar de nanomedicina que inclui pesquisadores com formação em biologia tumoral, genética, fisiologia, farmácia, medicina veterinária, biofísica, física, física medica e química, o professor e seu grupo participam ativamente de eventos científicos que reúnem diversos profissionais, inclusive médicos com várias especializações que já utilizam a hipertermia em humanos para tratamento do câncer. “Estes contatos científicos são fundamentais em áreas de interface como a que nosso grupo atua”, conclui Bakuzis.
A pesquisa que gerou o artigo na Nanoscale recebeu financiamento do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) e da Fundação de Amparo à Pesquisa do Estado de Goiás (FAPEG) e foi realizada como parte do trabalho de doutorado de Marcus Carrião dos Santos.

PAULO HENRIQUE DIAS
Parabéns a todos os envolvidos nestas pesquisas, sem sombra de dúvidas estão no caminho certo, gostaria de saber se já existe algum centro realizando esse tratamento no Brasil, e se não o que seria preciso para começar.
Andris Bakuzis
Prezado Ebert
Obrigado pelas observações e perguntas. Na literatura costuma-se ouvir que ao chegar em determinada temperatura pode-se aniquilar células tumorais. No entanto, a situação é mais complexa. De fato pesquisadores desta área, Medicina Térmica, já sabem que o relevante é o que chamamos de dose térmica. Neste caso não só a temperatura mas o tempo de permanência nesta temperatura, que é relevante para o tratamento por meio de entrega de calor.
Dito isto, talvez seja importante comentar que pode-se localizar radiação eletromagnética (não-ionizante) em órgãos específicos ou pequenas regiões (mas infelizmente até o momento não em qualquer região do corpo). Algumas estratégias invasivas, como equipamentos de ablação por RF ou microondas, já estão em uso na medicina há algum tempo.
Por outro lado, equipamentos que fazem esta entrega de forma não-invasiva também já foram aprovados pela FDA para uso em seres humanos, seja para tratar tumores superficiais (sem uso de nanotecnologia), ou ainda outros, como um recente desenvolvimento de uma empresa européia, que possui um equipamento que consegue localizar num volume de interesse campos magnéticos capazes de, ao interagir com nanopartículas magnéticas, gerar calor suficiente para auxiliar no tratamento do câncer. Este equipamento está aprovado para uso em conjunto, i.e. a braquiterapia e hipertermia no tratamento de tumores do cérebro.
Esta terapia conjunta, aonde calor é associado a radioterapia (ou quimioterapia), pode sim auxiliar na diminuição de efeitos colaterais. Na verdade já se sabe por meio de estudos clínicos e pré-clínicos, que a dose pode reduzir consideravelmente ao se combinar calor a terapias tradicionais.
Portanto, é muito provável que no futuro próximo, além das terapias tradicionais outras estratégias, como esta de entrega de calor, possam ser acopladas de maneira mais usual para melhorar a qualidade de vida de pacientes com câncer.
Ebert Ribeiro Figueiroa
Se altas temperaturas podem causar câncer, como em bebidas acima de 60 graus centígrados, que temperatura seria a adequada para dissolução de tumores e como regular essa temperatura através dessas nanoparticulas, já que os meios, em diferentes partes do corpo, são diferentes? Todo trabalho que está sendo feito merece todos os esforços destes profissionais que estão trabalhando em conjunto para quem sabe uma possível cura para o câncer, que até a pouco, seria uma missão que quase impossível. Será? Este poderá ser a resposta e sem efeitos colaterais que acompanham a maior parte dessas terapias. Parabéns por todos estarem proporcionando mais esta esperança a comunidade.
Andris Bakuzis
Prezado Ebert
Notei agora também que esqueci de responder outra questão relevante apontada por você, a qual diz respeito a monitorar a temperatura dentro dos órgãos de maneira não-invasiva. Esta área de monitoramento da entrega de calor é muito importante neste tipo de tratamento. Atualmente, pode-se utilizar a técnica de ressonância magnética (RMNI) para monitorar tridimensionalmente esta entrega de calor na região de interesse (é possível usar também o ultrassom mas ainda parecem haver algumas limitações neste caso). Infelizmente, no caso das nanopartículas magnéticas, tal estratégia não pode ser usada, já que o calor depende da rotação dos momentos magnéticos das nanopartículas. Estas, por sua vez, dentro de um equipamento de RMNI, encontram-se de certa forma bloqueadas, já que o paciente entra dentro de um magneto permanente, ou seja há um campo magnético de alta intensidade dentro do RMNI que impede que sob ação de um campo oscilante haja rotação dos seus momentos magnéticos. Portanto, impossibilita a geração de calor. Novas alternativas não-invasivas estão sendo pensadas para resolver esta questão, mas até o momento no tratamento de pacientes, isto ainda é feito majoritariamente por meio da inserção de termômetros de fibra óptica no paciente.